セリアック病は、グルテンの成分であるグリアジンを、免疫がからだに有害なものと認識し、グリアジンが付着した小腸の細胞を攻撃し、破壊することで起きます。症状は小腸だけでなく、全身に現れます。患者さんは人口の 1 %といわれていますが、近年、増加傾向にあります。患者さんは、一生涯、グルテンフリー食を摂り続ける必要があります。
セリアック病ってどんな病気?
セリアック病の発生機序
人間は、自分のからだを守るために免疫という仕組みを持っています。有害な物質がからだの中に入ると、それを認識して攻撃することで、有害な物質を排除します。
小麦、大麦、ライ麦に含まれるたんぱく質であるグルテンには、グリアジンという成分が含まれますが、免疫がこのグリアジンを有害なものと認識し、それを攻撃することがきっかけで起きる病気が、セリアック病です。
このように自分の免疫が誤って自分のからだを傷つけてしまう病気を、自己免疫疾患といいます。
グリアジンがからだに入ると、セリアック病の人はグリアジンを排除するために T細胞 という免疫細胞の働きが活発になります。T細胞はもともと、ウイルスや細菌に感染した細胞やがん細胞を見つけて、殺す働きをするものです。セリアック病の人は、本来は有害ではないグリアジンを見つけ、グリアジンが付着した小腸の粘膜を破壊してしまいます。
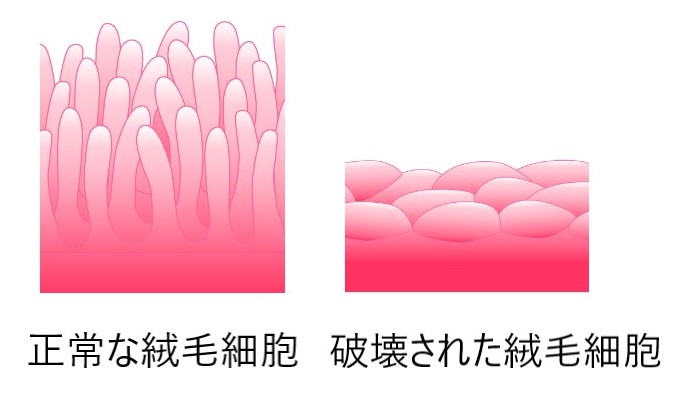
人間が、栄養分の 90 % を、小腸で吸収します。そのため、小腸の粘膜は絨毛細胞といわれる細かいひだ状になっており、ひだの部分を全部広げると、テニスコート 1 面分にもなります。
セリアック病の人がグルテンが含まれる食べものを摂ると、T細胞がグルテンが付着した絨毛細胞を破壊するため、ひだがなくなってしまいます。その結果、必要な栄養分が吸収できなくなるとともに、粘膜に穴が開いてしまい、本来吸収されるはずのない物質が、体内に入ってしまいます。その結果、次に示すような症状が起きます。
セリアック病の症状
消化器症状
絨毛細胞が破壊されることで、たべものの成分が吸収されずに腸内に残ってしまうため、軽度、かつ間欠性の下痢が起きます。特に、脂肪の吸収率が下がるため、脂肪が多く含まれる便(脂肪便)が見られます。
健康な人の便に含まれる脂肪量は 1 日 2 g 程度ですが、セリアック病では1 日 7~50 g という高い濃度の脂肪便が見られるのが特徴です。
皮膚症状
疱疹状皮膚炎といって、強いかゆみを伴う水疱性丘疹が、肘、膝、殿部、肩、および頭皮の側面に対称性にできます。これは本来は体内に入ることがないグリアジンの成分が、穴が開いた小腸から体内に入り、血液によって皮膚まで運ばれて、そこでアレルギー反応を起こすことが原因と考えられています。
全身症状
必要な栄養分、特にビタミンやミネラルの吸収率が下がるため、倦怠感、筋力低下、食欲不振、体重減少、貧血、舌炎、口角炎、アフタ性潰瘍、ビタミン D 欠乏症、カルシウム欠乏症、月経の停止が起こります。
なお妊孕性の低下(不妊症)については、論文でその可能性が否定されているので、削除しました 1)。
食べものに含まれるグルテンが直接の原因なんだから、消化器症状がまず現れるはず、と考えがちですが、最近の研究で、消化器症状が見られないセリアック病がかなりの割合で存在することがわかっています。

セリアック病の発症要因
生まれたときからセリアック病を患っていることは少なく、突然、発症すると考えられています。花粉症をイメージしていただくと、わかりやすいかもしれません。
セリアック病の発症には、遺伝的な要因、グルテンによる暴露、環境要因の 3 つが必要といわれています 2)。グルテンを含む食事を食べ始めた時期と、将来のセリアック病の発症との関係は、よくわかっていません。
環境要因としては、胃腸の感染症、投薬、α-インターフェロンの投与、手術がきっかけとなって、セリアック病が発症することがわかっています。一方、セリアック病の女性の 15〜20 % は、出産後の産褥期に重篤な症状が発生する可能性があるといわれています。
セリアック病の患者数
セリアック病の存在が知られるようになってから、まだ 50 年ほどしか経っていません。
セリアック病の診断基準も 2013 年にできましたが 3)、これに当てはまらないセリアック病があることも、最近になってわかってきました。セリアック病の人がどれくらいいるのかについても、正確な数字はわかっていません。たた、これまでの研究結果をまとめた最新の論文によると、患者数について、次のようなことがわかっています 4)。
・血液検査の結果に基づくと、人口の 1.4 %。
・十二指腸の細胞を採取した検査(生検)の結果に基づくと、人口の 0.7 %。
・地域別では、ヨーロッパとオセアニアで人口の 0.8 %、アジアで 0.6 %、アフリカと北アメリカで 0.5 %、南アメリカで 0.4 %。
・性別では、女性の 0.6 %、男性の 0.4 %
・年齢別では、こどもの人口の 0.9 %、成人の人口の 0.5 %
つまり、おおよそ 100 人 に 1 人くらいと考えて間違いないでしょう。
ところで日本では、次の 2 の理由から、セリアック病の患者さんは少ないといわれてきました 5)。
- セリアック病の人が持つといわれる白血球の血液型 HLA を持つ人が少ないこと。
- グルテンを含む食品の摂取量が、欧米に比べて少ないこと。
まず、白血球の血液型 HLAについて説明します。
血液型にはA、B、O、ABの 4 つがありますが、これは赤血球の血液型です。白血球にも血液型があり、このうち、HLA-DQ2 または HLA-DQ8 の少なくとも一つの型を持つ人が、セリアック病になりやすいといわれています。日本人はこの血液型を持つ人が、欧米人より少ないのです。
しかしこれについては、2021 年に驚くような論文が出ています 6)。日本で、セリアック病として診断された人の HLA検査 を行ったところ、HLA-DQ2、HLA-DQ8のいずれの型も持っていなかった、というのです。この論文によると、日本のセリアック病は、米国やヨーロッパのセリアック病とは異なる遺伝的および免疫学的特徴を持っている可能性があるとのことです。
一方、日本でセリアック病の人がどれくらいいるか調査した例が、一つだけあります 7)。2008~2013 年に、島根県の 4 つの地域で健康診断を受けた 2055 人の成人から集めた血清サンプルを使って、セリアック病の抗体検査を行いました。その結果、0.19 % がセリアック病の可能性があるという結果が得られたというものです。
しかし、この調査の結果から、日本のセリアック病の患者数は、人口の 0.19 % だというのは、早計です。まず、健康診断を受けた人の年齢の中央値が、67.0 歳でした。次に対象者の居住値は、出雲市、雲南市、大南町、隠岐の島町という、都市化が進んでいない(= 和食中心の食生活である可能性が高い)地域でした。さらに この検査では、7 年以上も前の血液サンプルを使っていました。
結局、日本にセリアック病の人がどれくらいいるのかについて、信頼できる情報は存在しません。

セリアック病は増加傾向
セリアック病の人の数は、過去 50 年間で 4~5 倍に増加したことが、保存されていた血清を使った研究から明らかになっています 1)。衛生環境がよくなったため、微生物抗原への曝露が減ったことが理由として指摘されていますが、はっきりしたことはわかっていません。
また、セリアック病の患者数が、おとなが人口の 0.5 %であるのに対し、こどもが人口の 0.9 %であることから、増加傾向にあることがわかります。乳児期に発症した小麦アレルギーの 63 %は、3 歳の時点でアレルギー症状を示さなくなりますが、セリアック病は一度発症すると、治ることはありません。セリアック病のこどもは、数十年後にはおとなになります。
日本では、セリアック病は極めてまれな病気といわれていましたが、米国国立医学図書館(National Library of Medicine)が運営する医学・薬学系文献のデータベースである PubMed で、“celiac disease” & “japan” というキーワードで検索して、ヒットした論文の抄録を読んだところ、日本でもセリアック病に関する研究論文が 20 件ほどありました。出版された年を見ると、2021 年が 5 件、2020 年は 2 件、2019 年は 3 件と、この 5 年間に集中しています。つまり、日本でもセリアック病と診断される人が増えてきているようです。
セリアック病の検査と診断基準
セリアック病の検査は、血液中にセリアック病特有の抗体が存在するか調べる血液検査と、十二指腸の細胞を取り出して、細胞壁の絨毛が損傷していないか調べる生検の二本立てです。症状などから判断して、セリアック病である可能性が高い場合と、低い場合とで、検査方法が異なります。これは可能性が低いにもかかわらず、時間と費用のがかかり、からだへの負担が大きい検査を行うことを避けるためです。
さまざまな検査方法と、アメリカ消化器病学会が公表している診断基準を紹介します 3)。
セリアック病の検査
抗組織トランスグルタミナーゼ抗体検査(tTG-IgA 検査)
セリアック病になると、抗組織トランスグルテミナーゼというたんぱく質に対する IgA 抗体が血液中に産生されるので、血液中の抗体量を調べます。感度も特異性も 95 % と高く、コストも安いことから、まず最初に行われる検査です。
十二指腸生検
小型のカメラを備えた長いチューブを、口から小腸の上部まで入れて観察するとともに、十二指腸下降脚のから小さな組織サンプルを採取し(これを生検といいます)、細胞壁の絨毛が損傷していないか調べます。
抗組織トランスグルタミナーゼ抗体検査(tTG-IgG 検査)
抗組織トランスグルテミナーゼというたんぱく質に対する IgG 抗体の量を調べます。人によっては IgA 抗体の量が少ない場合があるので、試験の開始時に総 IgA 量を測定して、IgA 量が十分でない場合は、このテストも組み込まれます。
脱アミド化グリアジンペプチド抗体検査(DGP-IgG 検査)
脱アミド化グリアジンペプチドというたんぱく質に対する IgG 抗体の量を調べます。tTG-IgG 検査と同様、人によっては IgA 抗体の量が少ない場合があるので、試験の開始時に総 IgA 量を測定して、Ig A量が十分でない場合は、このテストも組み込まれます。
遺伝子検査
血液中の白血球の型を調べます、赤血球に、A 型、 型、AB 型、O 型といった血液型があるのと同様、白血球にも血液型があります。白血球抗原(HLA)に DQ2 もしくは DQ8 という型があるかどうか調べます。セリアック病の人の 99 % は、HLA-DQ2 または HLA-DQ8 いずれかの型を持つことがわかっています。
なお、筋内膜抗体検査(EMA-IgG検査)は、セリアック病を見分ける精度は 99 %以上と最も高いですが、血清 tTG IgA 検査よりも費用が高く、測定に時間を要し、偽陰性になる可能性があるため、行われなくなりました。
セリアック病の診断基準
セリアック病である可能性が 5 %を超える場合
十二指腸生検と血液検査(抗組織トランスグルタミナーゼ抗体検査(tTG-IgA検査))を行い、
- ともに陽性 → セリアック病
- ともに陰性 → セリアック病ではない
- いずれかが陽性 → 遺伝子検査、tTG-IgG 検査、DGP-IgG 検査を行い判断
セリアック病である可能性が 5 %以下の場合
十二指腸生検は行わず、血液検査のみ行います。
まず、抗組織トランスグルタミナーゼ抗体検査(tTG-IgA検査)と総 IgA 量を調べます。
- tTG-IgA検査が陽性 → 十二指腸生検を行います。あとは、上記と同じ。
- tTG-IgA検査が陰性で、総IgAが少ない → 追加でtTG-IgG 検査、DGP-IgG 検査を行い判断します。
- tTG-IgA検査が陰性で、総IgAが少ない → セリアック病ではない

セリアック病の治療法
セリアック病には根本的な治療法はありません。唯一の対処法は、生涯にわたってグルテンを含まない食事を摂ることです 8)。
ただ実際のところ、グルテンフリー食品は。全くグルテンを含んでいないわけではありません。どれくらいのグルテンなら許容されるのかについては、個人差があります。グルテンフリー食に変えていたとしても、1 日わずか 50 mg のグルテンの摂取で、セリアック病の症状が再発する可能性があります。
また、セリアック病であるにも関わらず、グルテンフリー食を摂らず、グルテンが入った食事を続けた場合、グルテンフリー食にしたグループと比べて、死亡率が 4~5 倍高いという報告もあります。
またセリアック病と診断された前後において、グルテン摂取量が多い人ほど、セリアック病による死亡率が増加することがわかっています。
まとめ
- セリアック病は、グルテンの成分であるグリアジンをからだに有害なものと認識して、グリアジンがある小腸の細胞を自分の免疫が攻撃することで起こる。
- その結果、小腸の絨毛細胞が破壊され、必要な栄養分が吸収できなくなるとともに、本来吸収されるはずがない物質が体内に入ってしまうことで、消化器症状、皮膚症状、全身症状が現れる。
- セリアック病は、なんらかのきっかけで、人生のいつでも発症する可能性がある。
- セリアック病の患者数は、人口の 1 %程度と考えられている。しかも、セリアック病の患者数は増加傾向にある。
- セリアック病かどうかは、血液中にセリアック病特有の抗体が存在するかどうかを調べるとともに、十二指腸の細胞を取り出して、細胞壁の絨毛が損傷していないか調べる。
- セリアック病の唯一の治療方法は、生涯にわたってグルテンを含まない食事を摂ることである。
参考文献
1) Lebwohl B, Ludvigsson JF, Green PH. Celiac disease and non-celiac gluten sensitivity. BMJ. 2015; 351:h4347. Published 2015 Oct 5. doi: 10.1136/bmj.h4347
2) Al-Toma A, Volta U, Auricchio R, et al. European Society for the Study of Coeliac Disease (ESsCD) guideline for coeliac disease and other gluten-related disorders. United European Gastroenterol J. 2019; 7(5):583-613. doi: 10.1177/2050640619844125
3) Rubio-Tapia A, Hill ID, Kelly CP, Calderwood AH, Murray JA; American College of Gastroenterology. ACG clinical guidelines: diagnosis and management of celiac disease. Am J Gastroenterol. 2013; 108(5):656-677. doi: 10.1038/ajg.2013.79
4) Singh P, Arora A, Strand TA, et al. Global Prevalence of Celiac Disease: Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol. 2018; 16(6):823-836.e2. doi: 10.1016/j.cgh.2017.06.037
5) Hokari R, Higashiyama M. Extremely low prevalence of Celiac disease in Japan: Eternal silence or just the calm before the storm?. JGH Open. 2020; 4(4):554-555. Published 2020 Aug 7. doi: 10.1002/jgh3.12352
6) Hayashida S, Murakami T, Tsuyama S, et al. Nihon Shokakibyo Gakkai Zasshi. 2021; 118(7):661-670. doi: 10.11405/nisshoshi.118.661
7) Fukunaga M, Ishimura N, Abe T, et al. Serological screening for celiac disease in adults in Japan: Shimane CoHRE study. JGH Open. 2020; 4(4):558-560. Published 2020 Apr 7. doi:10.1002/jgh3.12334
8) Rubin JE, Crowe SE. Celiac Disease. Ann Intern Med. 2020; 172(1):ITC1-ITC16. doi: 10.7326/AITC202001070